 La laminitis, también conocida como infosura, es una enfermedad caracterizada por la inflamación de la lámina podal. El proceso se desarrolla como consecuencia de desequilibrios vasculares que se traducen en una deficiente perfusión capilar en el interior del casco, comunicaciones arteriovenosas (anastomosis), isquemia, necrosis de la lámina podal y consecuentemente dolor. Es un proceso patológico multifactorial y multisistémico.
La laminitis, también conocida como infosura, es una enfermedad caracterizada por la inflamación de la lámina podal. El proceso se desarrolla como consecuencia de desequilibrios vasculares que se traducen en una deficiente perfusión capilar en el interior del casco, comunicaciones arteriovenosas (anastomosis), isquemia, necrosis de la lámina podal y consecuentemente dolor. Es un proceso patológico multifactorial y multisistémico. Esta patología no es consecuencia de un proceso local, sino que se debe a desórdenes metabólicos sistémicos, donde están involucrados el sistema cardiovascular, renal y endocrino, así como alteraciones de la coagulación sanguínea y del equilibrio ácido-base.
Etiofisiopatología
Las causas que conducen al desarrollo de la laminitis son múltiples y variadas; la enfermedad se desencadena cuando el animal entra en contacto con alguno de los factores que se consideran desencadenantes: sobreingestión de cereales, ingestión de gran cantidad de agua fría, obesidad e ingestión de pastos frescos, cólicos, infecciones sistémicas (neumonías, endometritis), confusiones en el casco, errores yatrogénicos, alergias a determinados fármacos, yeguas con diestros o estros prolongados, retención de secundinas, etc. Aunque cualquiera de ellos aisladamente puede provocar la enfermedad, también es frecuente la asociación de varias causas.
El factor etiológico más importante y que causa laminitis con mayor frecuencia, es la ingestión de cereal en cantidad superior a la que el animal puede tolerar, ocurre tanto en animales que diariamente reciben una ración de grano, como en aquellos que de manera accidental ingieren dicha cantidad. Los cereales implicados son el maíz, la cebada y el trigo; la sobrecarga de avena no suele desencadenar cuadros de laminitis.
El grano es rico en carbohidratos, por lo que al ingerir el animal una gran cantidad de estos cereales se produce una sobrecarga de carbohidratos, como consecuencia ocurre una disbiosis de la flora bacteriana cecal, de modo que se desarrollan fermentaciones lácticas por bacterias como los Estreptococos y los Lactobacillus fundamentalmente, que aumentaron su número en detrimento de la flora bacteriana nativa cecal. Al aumentar la concentración de ácido láctico en el ciego, se produce un descenso de pH, lo que conduce a la destrucción de las bacterias Gram, con la consecuente liberación de sus endotoxinas (componentes lipopolisacáridos vasoactivos). Por otra parte, el aumento de la concentración de ácido láctico, junto con el descenso del pH, provocan la destrucción de la mucosa intestinal, abriendo de este modo camino a las endotoxinas hacia la circulación sistémica.
Se instaura un cuadro de endotoxemia dando lugar a un conjunto de fenómenos tanto sistémicos como locales. Se ha propuesto que las endotoxinas actúan como mecanismo disparador de la laminitis, se sabe que activan la cascada de la coagulación directamente a través del factor de Hageman (Factor XII; participa en la vía intrínseca de la coagulación, en la activación de la fibrionolisis y en el sistema de cininas plasmáticas). Dado que se activa mediante el contacto con superficies no endoteliales y extrañas (p.ej. endotoxinas), se denomina factor de contacto y constituye la fase inicial de la coagulación plasmática por vía intrínseca, además causan daño en las células endoteliales y promueven la agregación plaquetaria, de modo que se instaura un perfil hemático compatible con la coagulación intravascular diseminada (CID); como consecuencia, inicialmente se produce una vasoconstricción periférica provocando una disminución de la perfusión del lecho capilar del casco y cierto grado de isquemia. La agregación plaquetaria y la formación de microtrombos en el lecho capilar del casco contribuyen a mantener la isquemia por oclusión vascular; además, se libera a partir de las plaquetas el tromboxano A2, que es un potente vasoconstrictor, que favorece aún más el proceso. Al mismo tiempo comienza la respuesta inflamatoria por la liberación de autacoides, como la histamina, serotonina, bradiquinina, prostanoides (PG I2 y PG E2), leucotrienos e interleukina 1. La histamina desarrolla un papel muy importante en la inflamación aguda, su acción es vasodilatadora en las arteriolas pero su papel más importante en la inflamación es indirecto ya que potencian la acción de otros mediadores como la histamina y la bradicinina, produciendo dilatación arteriolar, mayor permeabilidad capilar e hiperalgesia. El leucotrieno B4 interviene en el paso de los leucocitos al exudado inflamatorio.
Así, por una parte existe un cierto grado de necrosis tisular de la lámina dérmica podal debido a la isquemia hística; debido a la inflamación se produce vasodilatación arteriolar y dolor periférico, este dolor periférico provoca la estimulación de las glándulas adrenales que, como respuesta liberan catecolaminas y esteroides, al mismo tiempo que en el riñón se activa el sistema renina-angiotensina, resultando en conjunto vasoconstricción e hipertensión sistémica, debido a lo cual aumenta el flujo sanguíneo en las extremidades.
Como en el casco la perfusión capilar es mínima por los problemas ya citados, se producen anastomosis arteriovenosas entre las arteriolas y las vénulas dilatadas, soslayándose así el lecho capilar del casco. Debido a la permeabilidad de las arteriolas se produce edema tisular rico en proteínas, que contribuye a aumentar todavía más la tensión en el interior del casco potenciándose la necrosis de la lámina podal. El resultado final es la muerte del tejido que une la tercera falange al casco, con lo que se produce rotación de ésta en el interior del estuche córneo.
Otras causas que con menor frecuencia causan infosura, son:
-la ingestión abundante de agua fría tras el ejercicio. Se piensa que la gastroenteritis o colitis resultantes estarían ligadas al desarrollo de la enfermedad.
-Contusiones en el casco, como consecuencia de traumatismos durante trabajos fuertes o sobre superficies muy duras, en especial en caballos con casco débil. Se desarrolla una osteitis podal y hematoma plantar, que si persiste desencadenaría en infosura.
-Infecciones sistémicas como neumonías, endometritis o metritis por retención placentaria. El mecanismo fisiopatogénico sería similar al ya descrito por un cuadro de endotoxemia.
-La obesidad y la ingestión de pastos frescos están ligados a cuadros de infosura. Es común en caballos que pastan en pastos de verano por ingestión de hierba o leguminosas con abundantes estrógenos que conducen a cuadros de obesidad. Generalmente se produce en caballos obesos como los ponies Shetland y Welsh, y en general en cualquier raza pesada. El desequilibrio hormonal podría ser la causa que desencadenaría en estos animales la infosura.
-En yeguas con diestro o estros prolongados. Se piensa que el desarrollo de la infosura estaría ligado a desequilibrios, pero no ha sido estudiado en profundidad.
-Los errores yatrogénicos incluyen la administración de altas dosis de corticosteroides. También se puede desarrollar infosura por fenómenos alérgicos tras la administración de determinados fármacos.
Sintomatología
Clásicamente la infosura se divide desde el punto de vista sintomático en dos bloques marcadamente diferenciados: infosura aguda e infosura crónica. Con total independencia de los factores etiológicos que desencadenan la infosura, las manifestaciones clínicas a nivel local son comunes.
Infosura aguda
Lo más frecuente es que se afecten los dos miembros anteriores, sin embargo, pueden verse afectadas las cuatro extremidades. La causa de la mayor incidencia de infosura en los miembros anteriores es parcialmente desconocida y se atribuye a factores biomecánicos. Si la infosura es debida a una contusión, sólo se afectará la extremidad traumatizada.
Cuando están afectadas las cuatro extremidades, el animal tiende a estar tumbado durante largos períodos de tiempo; en estación sitúa los pies cranealmente (metidos bajo el vientre) y las manos caudalmente (metidas bajo el pecho), con el fin de reducir la superficie de apoyo y consecuentemente el dolor. Cuando están afectadas exclusivamente las extremidades anteriores, el animal sitúa éstas cranealmente con el fin de descargar mayor peso sobre los talones, además se muestra reacio a caminar.
Obel clasificó la infosura en cuatro grados según la sintomatología clínica:
Grado 1.- En estación el animal eleva alternativa y constantemente las extremidades. La cojera no es evidente al paso, pero el trote aparece acortado.
Grado 2.- El animal acorta el paso, se le puede elevar una extremidad pero con dificultad.
Grado 3.- El animal se mueve con dificultad resistiéndose a elevar las extremidades.
Grado 4.- El animal sólo se mueve si se le obliga.
La fase aguda se caracteriza por aparición repentina de cojera, se hace más evidente sobre una superficie dura o cuando se fuerza al animal a caminar en círculos. Generalmente la cojera se presenta entre las 16 y 24 horas posteriores a la sobreingestión de los cereales.
Normalmente el propietario no suele darse cuenta hasta que la infosura es de grado 3, cuando se ha producido degeneración de la lámina. Muchos animales presentan ansiedad, temblores musculares, taquipnea e hipertermia durante los primeros momentos. Las mucosas pueden aparecer congestivas, y es característico el calor en el borde del casco y pulso a nivel de las arterias digitales palmares.
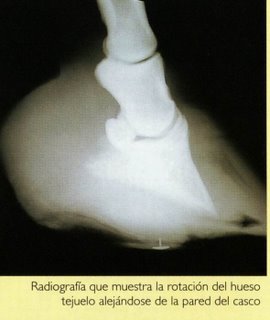
El edema producido entre la pared del casco y la tercera falange o hueso tejuelo produce el desplazamiento caudal de la misma, dando lugar a su rotación y hundimiento. Cuando se presenta el hundimiento de la falange se forma una especie de cavidad sobre el borde coronario, que en casos muy graves puede llegar a provocar la apertura del mismo, lo que indica una importante desvitalización producida por la isquemia; finalmente, el proceso puede agravarse por la entrada de gérmenes a través de la herida.
Durante el desarrollo de la infosura puede aparecer anorexia y depresión, dolor abdominal, diarrea, así como metritis, cólico, fallo renal agudo e incluso la muerte.
Cuando la cojera se mantiene más de 48 horas o cuando se aprecia evidencia de rotación de la tercera falange, se habla de infosura crónica.
Tratamiento
El tratamiento tiene dos objetivos. Primero, intentar aumentar el suministro de sangre a las láminas mediante la dilatación de los vasos sanguíneos usando bien acetilpromazina o clenbuterol por vía oral. Segundo, proporcionar un apoyo al hueso tejuelo a través de la ranilla en un intento de detener la rotación o el hundimiento. Para ello pueden usarse herraduras de corazón o plantillas de goma para la ranilla. En todos los casos se han de recortar bien los cascos. Para los casos de laminitis, la mejor cama es la de arena. Hoy en día también se usan virutas de papel. Los analgésicos son necesarios, a veces en dosis altas. Los caballos que contraen laminitis recurrente en pastos abundantes, se benefician de la virginiamicina oral que rebaja la producción de endotoxinas. Es esencial que tenga reposo absoluto en la cuadra. El ejercicio forzado que se recetaba antiguamente para los casos de laminitis era completamente erróneo ya que debilita la sujeción del tejido laminar aún más.
El pronóstico es siempre reservado (desconocido), especialmente si la radiografía muestra rotación del hueso tejuelo. La recuperación completa puede tardar meses. Además, el hecho de que el caballo parezca sano, no significa que el tejido laminar se haya recuperado completamente.
 Frecuentes son las dudas y mitos sobre el ciclo ovárico (o estral) de las yeguas. En este apartado, intentaremos ofrecer una información correcta y que sea útil para todos aquellos que desean iniciarse algún día en este apasionante mundo de la cría y reproducción equina.
Frecuentes son las dudas y mitos sobre el ciclo ovárico (o estral) de las yeguas. En este apartado, intentaremos ofrecer una información correcta y que sea útil para todos aquellos que desean iniciarse algún día en este apasionante mundo de la cría y reproducción equina. El ciclo ovárico en la práctica
El ciclo ovárico en la práctica






.JPG)